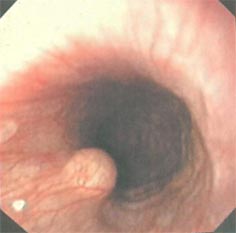
 Рак пищевода (видеоролик 8) представляет собой злокачественную опухоль, которая возникает из плоского эпителия слизистой оболочки пищевода, а в нижней трети пищевода формируется, вероятно, из железистого эпителия на фоне пищевода Барретта. Рак пищевода (видеоролик 8) представляет собой злокачественную опухоль, которая возникает из плоского эпителия слизистой оболочки пищевода, а в нижней трети пищевода формируется, вероятно, из железистого эпителия на фоне пищевода Барретта.
Аденокарцинома является наиболее частым гистологическим типом карцином дистальной части пищевода (примерно, 15% в год в США) и возникает на фоне пищевода Барретта. Так, на фоне дисплазии у лиц с пищеводом Барретта аденокарцинома формируется с частотой до 0,5 – 6% в год.
Курение сопровождается повышением риска аденокарциномы пищевода в меньшей степени, чем плоскоклеточного рака. Риск возникновения плоскоклеточного рака пищевода в 5—10 раз выше у курящих лиц по сравнению с не курящими. У курильщиков, которые злоупотребляют алкоголем, риск рака пищевода возрастает в 100 раз. Рак пищевода в большинстве случаев у больных относительно медленно прогрессирует. Смертность в течение первого года после подтверждения диагноза рака пищевода одна из самых высоких среди всех онкологических заболеваний. Средняя продолжительность жизни больных с III стадией заболевания без лечения не превышает 5—8 месяцев с момента уточнения диагноза. На ранних стадиях некоторые больные доживают до 6 лет даже без специального лечения, что встречается крайне редко.
Выделяют предраковые болезни и синдромы, изменения, состояния.
Пищевод Барретта, при котором происходит формирование цилиндрического эпителия в дистальных отделах пищевода является заболеванием - предшественником рака пищевода. Большинство случаев аденокарциномы пищевода возникает на фоне пищевода Барретта. Заболевание проявляется формированием цилиндрического эпителия в дистальных отделах пищевода. Цилиндрический метаплазированный эпителий кишечного типа имеет протяжённость от 3 см и более. Пищевод Барретта выявляют в 0,45-2,2% случаев при эзофагогастроскопии и в 10—20% случаев при эндоскопическом выявлении гастроэзофагеального рефлюкса. При пищеводе Барретта аденокарциномы пищевода развиваются в 40 раз чаще и с частотой 0,5 – 6% в год.
Химические ожоги пищевода, которые приводят не только к стриктурам, но и к раку пищевода даже через десятки лет. В большинстве случаев новообразования локализуются в средней трети пищевода.
Ахалазия, при которой происходят нарушения нормальной моторики пищевода, возникает патологический спазм нижнего пищеводного сфинктера. При ахалазии риск рака увеличен в 16- 30 раз.
Тилоз (неэпидермолитическая пальмоплантарная кератодермия) представляет собой редкое наследственное заболевание, которое передаётся по аутосомно-доминантному типу и характеризуется гиперкератозом ладоней и стоп, а также папилломами пищевода. При тилозе отмечают атипичный плоский эпителий и воспалительные процессы, которые приводят к раку пищевода у больных.
Синдром Пламмера-Винсона, при котором имеют место железодефицитная анемия, глоссит, спленомегалия (увеличение селезенки). Примерно, у 10% лиц с подобным синдромом возникает рак пищевода или рак нижней трети глотки.
Выявление дисплазии при гистологическом изучении биоптатов слизистой оболочки пищевода трактуется как предраковые изменения.
Клинические проявления у больных раком пищевода.
Следует отметить, что чаще отмечают смешанные формы роста рака пищевода, при которых обнаруживают элементы как экзофитного, так и эндофитного роста с ранним распадом опухоли и образованием изъязвления у больных, что определяет клинику.
К общим симптомам многие авторы относят слабость, утомляемость, снижение работоспособности, раздражительность, ухудшение или потерю аппетита, похудание, анемию, повышение температуры тела. На некоторых симптомах и синдромах остановимся ниже.
Дисфагия (часто) возникает после употребления твердой, а позже жидкой пищи. Дисфагия может проявляться чувством дискомфорта (покалывания) за грудиной, затруднением при глотании пищи и нарушением проводимости пищевода. Дисфагия проявляется, примерно, у 75% больных. Рак пищевода следует подозревать у любого больного с дисфагией.
Для появления дисфагии должно быть поражено 75% окружности органа.
Анорексия - потеря аппетита, отсутствие желания принимать пищу.
Похудание (часто) выявляют приблизительно у 60% пациентов, при котором обычно отмечают проявления дисфагии.
Одинофагия - боль при проглатывании пищи встречается у части лиц.
Боли возникают у 20% больных, которые могут быть самостоятельными или связанными с приёмом пищи. Боли могут быть постоянными или периодическими. Боль чаще возникает за грудиной или в подложечной области. Наличие болей в межлопаточной области может свидетельствовать о прорастании опухоли за пределы пищевода.
К особенностям опухолей нижнегрудного и абдоминального отделов пищевода можно отнести прорастание их чаще вверх по пищеводу. Представляет риск выход опухолевого роста за пределы стенки пищевода в среднегрудном отделе, что можно объяснить близостью трахеи, бронхов, сосудов корня легкого, дуги и нисходящего отдела аорты, верхней полой и непарной вен, когда возникает угроза прорастания опухоли в эти органы у больных.
Опухоль метастазирует в околопищеводные лимфатические узлы.
Диагностика рака пищевода.
Рентген - диагностика распространенного рака пищевода. К основным рентгенологическим симптомам рака пищевода относят ригидность стенок и нарушение рельефа слизистой оболочки в зоне поражения, «дефект наполнения», сужение просвета органа и супрастенотическое расширение. Труднее обнаружить опухоли малой распространенности с инфильтрацией только слизистой оболочки, иногда и подслизистого слоя органа. В подобных случаях уточнить диагноз помогут данные эндоскопии.
Компьютерная томография (КТ). КТ проводят с целью уточнения глубины опухолевой инфильтрации стенки пищевода, определения выхода опухоли за пределы пищевода, прорастания ее в соседние органы и кроме тог о для обнаружения метастатического поражения лимфатических узлов в средостении больных.
Фиброэзофагогастроскопия - эндоскопия слизистой оболочк пи щевода и желудка с прицельной биопсией слизистой оболоки пищевода или хромоскопия (эндоскопия после окраски слизистой оболочки пищевода) с прицельной биопсией слизистой оболоки пищевода.
Морфологическая диагностика позволяет проводить гистологическое изучение прицельно взятых биоптатов слизистой оболочки пищевода (при эндоскопии), при котором выявляют у больных рак пищевода в 90% случаев плоскоклеточный рак, а в 10% случаев - аденокарциному
Лечение больных раком пищевода (проводят онкологи, онкохирурги, подготовленные врачи эндоскописты для резекции или диссекции слизистой оболочки; планируют лечение с участием радиологов и химиотерапевтов). Выделяют цели лечения: радикальное удаление пораженного пищевода с лимфодиссекцией двух или трех региональных зон; паллиативное лечение, направленное на улучшение прохождения пищи по пищеводу и профилактику осложнений роста опухоли, который может продолжаться несколько месяцев, вероятнее всего.
Лечение больных раком пищевода включает в себя:
- диета № 1
- эндоскопическое лечение (эндоскопическая резекция или диссекция слизистой оболочки пищевода при ранней стадии - распространения опухоли в слизистой оболочке без инвазии)
– хирургическая резекция (при распространенном раке пищевода)
- эндолюминальная аблятивная терапия (алкогольная или лазерная при экзофитных опухолях при планировании эндоскопической паллиативной операции)
- установка эзофагеального протеза при эндофитных опухолях
- радиотерапия в неоперабельных случаях
- использование новых современных технологий
Следует остановиться на некоторых методах лечения больных раком пищевода.
Лучевая терапия. В неоперабельных случаях проводится радиотарапия. Так, лучевая терапия по радикальной программе в качестве самостоятельного метода возможна только при I стадии рака, обычно у неоперабельных больных. Назначают телегамматерапию, тормозное излучение и быстрые электроны. Суммарная доза достигает при этом 60—70 Гр. Внутриполостное облучение проводится путем введения радиоактивных источников в просвет специального зонда (эндостата), который устанавливают в просвет пищевода на уровне расположения опухоли больного. Плоскоклеточный рак обладает весьма высокой радиочувствительностью, и поэтому облучение может быть потенциально радикальным.
На практике, однако, возникает ряд труднопреодолимых проблем. Опухоль расположена очень глубоко, соседствует с крупными сосудами и бронхами. Облучение регионарных зон связано с повреждением жизненно важных чувствительных к ионизирующей радиации структур (легкие,сердце). Даже при использовании современной ротационной радиотерапевтической аппаратуры могут возникать тяжелые осложнения. Как правило, у большинства больных удается купировать симптомы дисфагии. Однако, больные быстро погибают от прогрессирования опухоли пищевода.
Медикаментозная терапия. Большинство больных раком пищевода обращаются с нарушением питания, снижением белков крови, обезвоживанием, что вынуждает использовать полноценное питание через рот жидкой пищей. Дополнительно внутривенно назначают кристаллоидные растворы, аминокислоты, жиры, углеводы, компоненты крови, витамины и другие лекарства.
Хирургическое лечение. Хирургическое лечение обычно проводится при распространенности рака в пределах Т1— Т2, а регионарное метастазирование определяют при этом только в пределах одного лимфатического коллектора (Nla). В последнее время торакальные и абдоминальные хирурги проводят одноэтапные операции, а безопасность обеспечивают адекватным доступом и формированием надежных анастомозов современным шовным материалом у больных.
Считают резекцию радикальной, когда проводимую с удалением не менее 8 см непораженного пищевода выше и 5 см ниже видимой границы опухоли. Хирургическое лечение рака пищеводасостоит из лечебного, восстановительного и реабилитационного этапов.
При локализации опухоли в нижней и средней трети пищевода проводят субтотальную резекцию с внутриплевральным анастомозом (операцию типа Льюиса) или экстирпацию грудного отдела пищевода с формированием анастомоза на шее больного.
Комбинированное лечение. Комбинированное лечение показано при раке пищевода II b—III стадии. Комбинированное лечение включает предоперационную химиолучевую терапию в сочетании с хирургическим лечением или хирургическое лечение с послеоперационной лучевой терапии. Больным с IV стадией рака выполняют паллиативное химиолучевое и симптоматическое лечение под контролем врача.
Прогноз
Из сведений литературы, летальность после радикальных и паллиативных резекций пищевода за последнее десятилетие снизилась до 2—3%. Выживаемость 5-летняя больных, которым проведена радикальная операция, составляет до 35-40% из сведений литературы.
Если послеоперационная лучевая терапия снижает частоту локальных рецидивов после радикальных операций с 35 до 20%, то выживаемость практически не увеличивается. Сочетание операции с облучением может стать источником специфических осложнений (кровотечение из трансплантата, лучевой фиброз легких) у больных.
После радикального лечения при I стадии рака пищевода 5-летняя выживаемость составляет более 90%, при II стадии — 50%, а при III стадии — до 10% из сведений литературы. При поражении регионарных лимфатических узлов прогноз значительно ухудшается. При этом, при распространенности N1 5-летняя выживаемость не превышает 18—20%, в то время как при отсутствии метастазов до 66% больных после радикального лечения имеют шанс прожить более 5 лет больные, что вынуждает искать новые методы и способы для лечению больных раком пищевода.
Профилактика рака пищевода.
Профилактика рака пищевода может включать в себя не только раннюю диагностику и лечение лиц с предраковыми заболеваниями и состояниями пищевода, но и профилактику предраковых заболеваний и состояний пищевода: рациональное питание; здоровый образ жизни; исключение и защита от внешних факторов; использование медикаментозных и немедикаментозных средств и современных технологий.
|